Методы обследования, лабораторные тесты и функциональные пробы
(учебное пособие) 2-е издание, переработанное и дополненное
Главные редакторы: академик И.И. Дедов член-корр. Н.Г. Мокрышева
Научные редакторы: академик Г.А. Мельниченко академик М.В. Шестакова академик В.А. Петеркова д.м.н. Е.А. Пигарова
Оглавление
ОСНОВЫ ЭНДОКРИНОЛОГИИ
СИНТЕЗ ГОРМОНОВ
ОЦЕНКА ФИЗИЧЕСКОГО И ПОЛОВОГО РАЗВИТИЯ
ПАЛЬПАЦИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
ОЦЕНКА СТЕПЕНИ ГИРСУТИЗМА
ГЛАЗНЫЕ СИМПТОМЫ В ЭНДОКРИНОЛОГИИ
ПЕРОРАЛЬНЫЙ ГЛЮКОЗОТОЛЕРАНТНЫЙ ТЕСТ
ЛИКИРОВАННЫЙ ГЕМОГЛОБИН HBA1C
МАТЕМАТИЧЕСКИЕ МОДЕЛИ ОЦЕНКИ УГЛЕВОДНОГО ОБМЕНА
ГИПЕРИНСУЛИНЕМИЧЕСКИЙ ЭУГЛИКЕМИЧЕСКИЙ КЛЭМП-ТЕСТ
ГИПЕРГЛИКЕМИЧЕСКИЙ КЛЭМП-ТЕСТ
РЕАКЦИЯ ГОРМОНА РОСТА НА ГИПЕРГЛИКЕМИЮ
ПРОБА С ИНСУЛИНОВОЙ ГИПОГЛИКЕМИЕЙ
(ИНСУЛИНОТОЛЕРАНТНЫЙ ТЕСТ)
СТГ-СТИМУЛЯЦИОННЫЕ ПРОБЫ В ДЕТСКОМ ВОЗРАСТЕ
ПРОБА С ЛЮЛИБЕРИНОМ
ПРОБА С СИНАКТЕНОМ
МАЛАЯ ДЕКСАМЕТАЗОНОВАЯ ПРОБА
(НОЧНОЙ ПОДАВЛЯЮЩИЙ ТЕСТ С 1 МГ ДЕКСАМЕТАЗОНА)
ПРАВИЛА СБОРА СУТОЧНОЙ МОЧИ НА СВОБОДНЫЙ КОРТИЗОЛ
СБОР СЛЮНЫ НА КОРТИЗОЛ
СЕЛЕКТИВНЫЙ ЗАБОР КРОВИ ИЗ НИЖНИХ КАМЕНИСТЫХ СИНУСОВ (НКС)
ПРАВИЛА СБОРА СУТОЧНОЙ МОЧИ НА МЕТАНЕФРИНЫ И НОРМЕТАНЕФРИНЫ
ПРОБА С СУХОЕДЕНИЕМ
ПРОБА С ГИПЕРТОНИЧЕСКИМ РАСТВОРОМ
ПРОБА С ДЕСМОПРЕССИНОМ
ПРОБА С ВОДНОЙ НАГРУЗКОЙ
ИНДЕКС МАССЫ ТЕЛА
ПРОБА С АЛЬФАКАЛЬЦИДОЛОМ
ПРОБА С КОЛЕКАЛЬЦИФЕРОЛОМ
ПРОБА С ГИПОТИАЗИДОМ
АЛЬДОСТЕРОН-РЕНИНОВОЕ СООТНОШЕНИЕ
МАРШЕВАЯ ПРОБА
ПРОБА С ДЛИТЕЛЬНЫМ ГОЛОДАНИЕМ
ПРОБА С ГЛЮКОНАТОМ КАЛЬЦИЯ
ПРОБА С КЛОМИФЕНОМ
ПРОБА С ХОРИОНИЧЕСКИМ ГОНАДОТРОПИНОМ У МУЖЧИН И ПОДРОСТКОВ
ПРОБА КАЗАНОВЫ
СИСТЕМА BETHESDA ДЛЯ КЛАССИФИКАЦИИ ЦИТОПАТОЛОГИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
СЦИНТИГРАФИЯ ВСЕГО ТЕЛА С 123I ИЛИ С 131I
СЦИНТИГРАФИЯ ПАРАЩИТОВИДНЫХ ЖЕЛЕЗ
СЦИНТИГРАФИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
СПИСОК СОКРАЩЕНИЙ
Основы эндокринологии
В.И. Кандрор, Г.А. Мельниченко
Клиницист, встречающийся в ежедневной практике с конкретными проявлениями эндокринного заболевания (например, гангреной стопы у больного сахарным диабетом или узловым образованием в щитовидной железе), может воспринимать основные принципы функционирования эндокринной системы, да и само понятие этой системы, как некую абстракцию, вряд ли способ- ствующую решению сиюминутной терапевтической задачи. Однако знание и учет таких принципов формируют базис клинических подходов, без которого лечение во многом остается эмпирическим и, соответственно, существенно менее эффективным.
Межклеточные, межорганные, межсистемные коммуникации являются необходимым условием существования многоклеточного организма. По сво- ей сути эти коммуникации выполняют регуляторные функции, осуществляя передачу сигналов, вызывающих усиление или угнетение тех или иных био- логических активностей клеток, органов и систем с целью наилучшей адапта- ции организма к меняющимся условиям внешней и внутренней среды.
В процессе эволюции у животных сформировались две основные комму- никационные, или регуляторные системы: нервная и эндокринная. Первую обычно сравнивают с телеграфной сетью, соединяющей с помощью прово- дов (нервных волокон) источник информации с местом ее получения и реа- лизации. Вторая, которая представляет собой не слишком жестко связанную группу подсистем, использует для передачи информации кровообращение, т.е. является «беспроволочной». Роль регуляторных сигналов в этой системе выполняют высокоспециализированные химические вещества — гормоны. Гормоны узнаются клетками-мишенями, которые в процессе своей диффе- ренцировки программируются на прием тех или иных (обычно сразу многих) гормональных сигналов и на специфические реакции на каждый из таких сиг- налов. Такое программирование заключается в появлении в клетках-мишенях рецепторов тех или иных гормонов. В результате клетки, органы и ткани ме- няют свои активности таким образом, что важнейшие параметры внутренней среды организма (например, уровень глюкозы в крови) очень быстро восста- навливают свое исходное значение. Иными словами, регуляторные эффекты эндокринной системы, как и нервной, обеспечивают постоянство внутренней среды организма — необходимое условие его существования.
Каждая из эндокринных подсистем (гипоталамо-гипофизарно-адреналовая, гипоталамо-гипофизарно-тиреоидная, регуляции роста и др.) построена по строго иерархическому принципу и внутри каждой из них существуют жесткие прямые и обратные регуляторные связи. Строго говоря, выделение анатомиче- ски обособленной эндокринной системы, состоящей из отдельных желез вну- тренней секреции, в определенной степени является анахронизмом, поскольку эндокринными функциями обладают все без исключения клетки и ткани орга- низма. Яркими примерами могут служить многочисленные гормоны желудоч- но-кишечного тракта, иммуноцитов, сердца, почек, жировой ткани и т.д.
Одна из характерных особенностей гормональной регуляции заключается в том, что любая физиологическая активность клеток контролируется антагонистически действующими стимулами. По-видимому, существование не- скольких (не менее двух) регуляторов, влияющих на одну и ту же функцию противоположным образом, т.е. усиливающих и ослабляющих ее, обеспечи- вает возможность более тонкого ее приспособления к потребностям момента, чем присутствие только одного стимула, эффект которого мог бы определять- ся лишь его количественным вариантом. Так, в центральном звене эндокрин- ной регуляции — гипоталамусе — вырабатываются не только либерины, уси- ливающие активность отдельных популяций клеток передней доли гипофиза, но и статины, тормозящие функции соответствующих клеток. Постоянство концентрации глюкозы в крови поддерживается не только модуляцией секре- ции инсулина, снижающего эту концентрацию, но и секрецией множества так называемых контррегуляторных гормонов (в первую очередь, глюкагона, а также катехоламинов, кортикостероидов, гормона роста), оказывающих про- тивоположное действие.
Когда организм в силу изменения состояния внешней или внутренней сре- ды начинает испытывать потребность в усилении или ослаблении активности той или иной группы клеток, специализированные эндокринные образова- ния (например, отдельные железы внутренней секреции) модулируют свою функцию (например, продуцируют повышенное количество определенного гормона) с тем, чтобы привести эту активность в соответствие с возникши- ми потребностями организма. Как только специфическое действие гормона на клетки-мишени удовлетворит эту потребность, нужда в его повышенной продукции отпадает. Совершенно необходимо, чтобы, выполнив свою зада- чу, эндокринная железа была бы проинформирована об этом и получила воз- можность вернуться в исходное состояние, а биологически активный гормон был бы своевременно удален из клеточного окружения. Это предполагает существование в эндокринной системе механизмов обратной связи. Именно такие механизмы позволяют приводить секрецию гормона в точное соответ- ствие с потребностями его тканей-мишеней. Следует подчеркнуть, что “точка равновесия” между тропными гормонами и гормонами органов- мишеней не является константой на протяжении всей жизни человека и может меняться с возрастом, например, в возрасте старше 70 лет нарастает некоторая рези- стентность к тиреоидным гормонам, и референс ТТГ повышается.
Различают несколько вариантов обратных связей в эндокринной системе. Непосредственная отрицательная обратная связь ставит скорость синтеза или секреции гормона в зависимость от концентрации продуктов метаболических процессов, регулируемых этим гормоном. Иными словами, сама реакция на гормон противодействует дальнейшей стимуляции эндокринной железы. На- пример, тиреотропный гормон (ТТГ) передней доли гипофиза усиливает про-дукцию клетками щитовидной железы тиреоидных гормонов [тироксина (Т4) и трийодтиронина (Т3)], а повышение уровня последних в крови тормозит се- крецию гипофизарного ТТГ. Таким образом, уровень тиреоидных гормонов в крови регулируется их действием на стимул, активирующий их собственную секрецию. Аналогичная непосредственная отрицательная обратная связь су- ществует между уровнем глюкозы в крови и секрецией инсулина β-клетками островков поджелудочной железы. Тормозя печеночную продукцию глюкозы и усиливая утилизацию сахара периферическими тканями, инсулин снижает его концентрацию в крови. Поскольку глюкоза служит основным стимулом секреции инсулина, снижение ее концентрации тормозит продукцию последнего.
Отрицательная обратная связь может быть и опосредованной. Так, тиреоид- ные гормоны тормозят секрецию ТТГ не только в силу своего прямого действия на тиреотрофные клетки аденогипофиза, но и путем ингибирования продукции гипоталамического тиреотропин-рилизинг гормона (ТРГ, тиролиберина). В за- висимости от количества промежуточных звеньев в реализации обратных связей различают ультракороткие, короткие и длинные обратные связи. Функционирование отрицательных обратных связей — один из основных кибернетических принципов — является необходимым условием поддержа- ния постоянства внутренней среды. Гораздо труднее понять биологический смысл положительных обратных связей, когда гормон выступает в роли сти- мула своей собственной продукции. Такого рода связи проявляются лишь в некоторых особых условиях. Классическим примером служит связь между яичниковым гормоном эстрадиолом и гонадотропными гормонами адено- гипофиза. Эстрадиол в определенной концентрации усиливает секрецию фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов ги- пофиза (непосредственная положительная обратная связь), равно как и про- дукцию гипоталамического гонадолиберина (опосредованная положительная обратная связь). Более того, секретируемый развивающимся фолликулом яич- ника эстрадиол способен прямо усиливать собственную продукцию за счет стимуляции синтеза яичниковых рецепторов гонадотропинов и повышения чувствительности яичника к этим гормонам.
Положительные обратные свя- зи грозят выходом ситуации из-под контроля («разносом» системы). Поэтому они отличаются внутренней нестабильностью и функционируют лишь в пре- делах определенных концентраций гормонов. При дальнейшем нарастании концентрации последних включаются классические отрицательные обратные недеятельности организма. Неудивительно поэтому, что такие связи бывают не только «наружными» (как в описанных ситуациях), но и «внутренними», т.е. замыкающимися внутри каждой клетки (например, торможение синтеза гормонов щитовидной железы йодидом, угнетение биосинтетических реак- ций их продуктами и т.п.). Еще один уровень замыкания обратных связей локализуется на этапе восприятия гормонального сигнала клеткой, т.е. на уровне клеточных рецепторов. Сам гормон (или лиганд) может регулировать количество или сродство своих собственных рецепторов. Обычно речь идет о так называемой «снижающей регуляции» (down-regulation), когда избыток гормона обусловливает уменьшение числа или сродства рецепторов (что ле- жит в основе феномена десенситизации ткани), однако возможна и «повы- шающая регуляция» (up-regulation), приводящая к сенсибилизации клеток к данному гормону.
В последние десятилетия само понятие эндокринологии претерпело прин- ципиальные изменения. В настоящее время разделение нервной и эндокринной систем представляется достаточно условным. Так, нейромедиаторы (на- пример, норадреналин) могут циркулировать в крови как гормоны, а продук- ция классических гормонов (таких как адреналин или инсулин) находится под влиянием нервных импульсов. Тесное взаимодействие нервной и эндокрин- ной систем особенно наглядно проявляется в гипоталамусе, в ядрах (скоплениях нейронов) которого вырабатываются многие химические передатчики. Гипоталамический гормон ТРГ, например, действует в центральной нервной системе как нейротрансмиттер. В головном мозге присутствуют также мно- гие другие гормонально активные соединения, включая стероиды (нейростероиды).
По традиции гормонами называют вещества, секретирующиеся в кровь определенными органами (эндокринными железами) и действующие на отда- ленные от места своей продукции ткани. Однако химические медиаторы вы- деляются далеко не только классическими эндокринными железами, но прак- тически клетками любых тканей организма. Некоторые химические передат- чики циркулируют лишь в ограниченных пространствах внеклеточной жид- кости, действуя на соседние клетки того же органа, такое действие называют паракринным (например, эффекты половых стероидов в яичниках). Иногда сигнальная молекула даже остается связанной с мембранной продуцирующей ее клетки, но взаимодействует с соседней (юкстакринное действие). Действие гормона на те же клетки, которые его продуцируют, называют аутокринным. Гормоны могут влиять на внутриклеточные процессы, и не покидая продуци- рующих клеток (интракринное действие). Примером аутокринных эффектов является ингибирующее влияние инсулина на свою собственную секрецию.
Традиционное представление об эндокринной системе ограничивается не- большим числом «классических» эндокринных желез. К ним относятся гипо- таламус, продуцирующий либерины и статины, которые регулируют секрецию гормонов передней доли гипофиза (аденогипофиза) — кортикотропина (АКТГ), тиреотропина (ТТГ), лютеинизирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, соматотропина (гормона роста, ГР) и пролактина (ПРЛ). За- дняя доля гипофиза (нейрогипофиз) служит хранилищем и местом выделения в кровь вырабатываемых в гипоталамусе антидиуретического гормона (АДГ, вазопрессина) и окситоцина. В головном мозге расположена и шишковидная железа (эпифиз), продуцирующая мелатонин. Классические периферические эндокринные органы включают щитовидную железу [тироксин (Т4), трийод- тиронин (Т3) и кальцитонин], околощитовидные железы (паратгормон, ПТГ), надпочечники (кортикостероиды и адреналин), яичники и яички (половые сте- роиды) и поджелудочную железу (инсулин, глюкагон, соматостатин).
В последние годы многие представления классической эндокринологии подверглись пересмотру. Выяснилось, например, что гормоны (от грече- ского hormao — побуждаю) могут обладать не только стимулирующим, но и ингибирующим влиянием на функции своих клеток-мишеней. Пришлось отказаться от концепций «одна железа — один гормон» или «один гормон — один ген». Во многих эндокринных железах одновременно синтезируют- ся несколько гормонов (щитовидная железа — тироксин и кальцитонин, под- желудочная железа — инсулин и глюкагон, и т.п.), а один и тот же гормон способен активировать (или ингибировать) функцию многих генов.
В сферу изучения эндокринологии оказались вовлеченными и витамины (витамин D), метаболиты (например, глюкоза и жирные кислоты) и даже газы (окись азо- та). Усиленно изучаются вырабатываемые “неклассическими железами гор- моны”, в том числе жировой тканью (лептин, резистин, висфатин, адипонек- тин), остеоцитами и остеобластами – остеокальцин, FGF23, клетками желу- дочно – кишечного тракта (ЖКТ) – грелин, глюкагоноподобный пептид и др. Уместно вспомнить удивительное прозрение Старлинга, назвавшего “гормоном” именно вещество , происходящие из клеток ЖКТ. Механизмы передачи сигналов в эндокринной системе во многом сходны с таковыми в иммунной системе. Иммунокомпетентные клетки продуцируют пептиды (интерлейки- ны, интерфероны и др.), действующие преимущественно пара-, ауто-, юкста- и интракринным путем.
Реализация обратных связей с центральными нервными структурами пред- полагает возможность проникновения продуктов эндокринных желез через гематоэнцефалический барьер (что зависит от размеров этих продуктов, их жирорастворимости, присутствия специфических переносчиков, механизмов активного транспорта и т.п.), а также наличие в центральной нервной системе специфических рецепторов периферических гормонов.
При рассмотрении действия гормонов необходимо учитывать, что они не инициируют новых реакций в клетках-мишенях, а лишь меняют скорость присущих этим клеткам реакций.
Классификация гормонов
По химической природе гормоны можно разделить на три большие груп- пы: белковые/полипептидные (б/п) гормоны, стероидные гормоны (с) и про- чие (п). Примеры гормонов каждой из этих групп вместе с их основными источниками приведены в таблице 1.
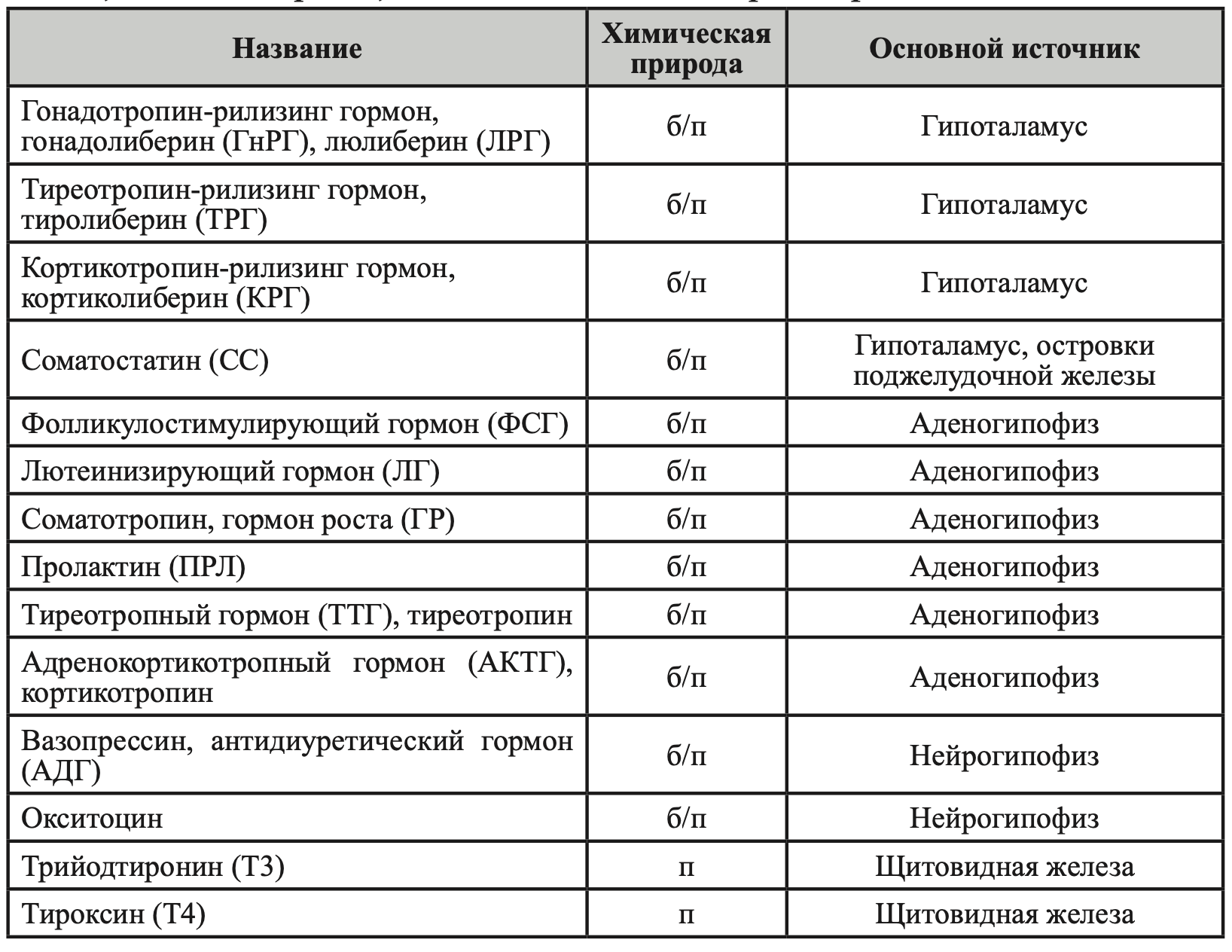
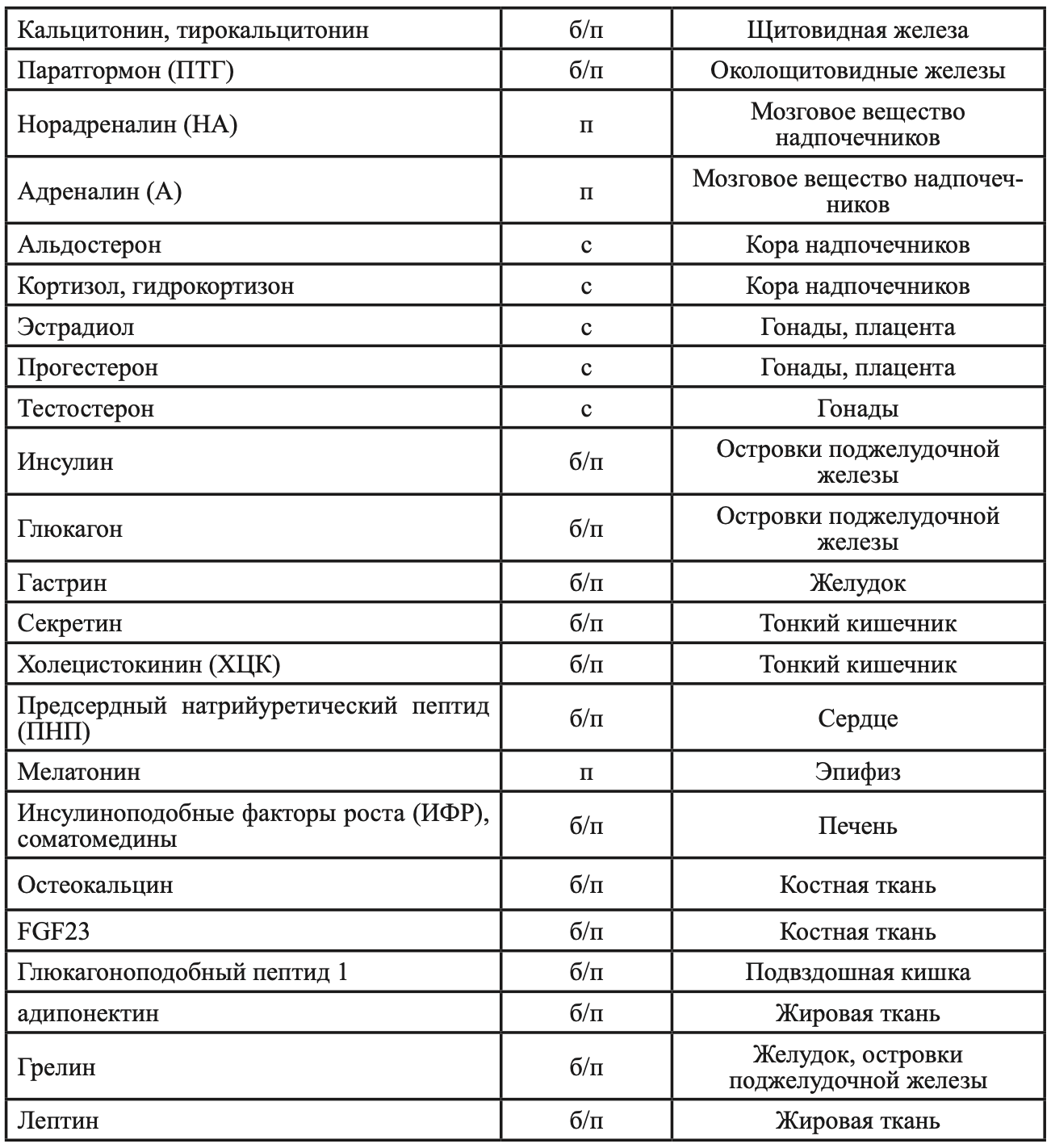
По Лейкок Дж.Ф., Вайс П.Г. Основы эндокринологии (пер. с англ.). М., Медицина, 2000.
Белковые и полипептидные гормоны состоят из аминокислот, соединенных пептидными связями. Большинство таких гормонов являются гликопротеинами, т.е. содержат углеводные остатки. К стероидным гормонам относятся продукты коры надпочечников (кортикостероиды) и половых желез (андрогены, эстрогены и прогестины), а также метаболиты витамина D (холекальциферола). Все они являются производными холестерина и содержат циклопентанпергидрофенантреновое ядро с различными боковыми цепями и группами, придающими специфичность разным молекулам). Смешанная группа гормонов включает производные аминокислот (йодированные тиронины, катехоламины, мелатонин) и длинноцепочечных жирных кислот (простагландины, тромбоксаны), а также другие молекулы, выступающие в роли химических передатчиков сигналов, например, окись азота (NO), которая присутствует в очень многих тканях (головном мозге, сосудистом эндотелии, клетках иммунной системы и др.). Разнообразные эффекты NO включают расслабление гладкой мускулатуры сосудов, угнетение агрегации тромбоцитов, цитотоксическое действие на многие микроорганизмы и др.
Гормональные подсистемы могут включать гормоны разных химических классов. Так, к гонадотропной системе относятся моноамины, олигопептиды, гликопротеины и стероиды. Аналогичные системы существуют и для регуля- ции многих других физиологических функций. Гормоны классифицируют и по источникам их образования — гормоны гипофиза, надпочечников, щито- видной или поджелудочной железы и т.п.
Продукция гормонов регулируется, как правило, на каком-либо из трех этапов: их синтезе, секреции или путем увеличения (уменьшения) числа и размеров эндокринных клеток.
Синтез гормонов
В.И. Кандрор, Г.А. Мельниченко
Белковые и полипептидные гормоны
Многие полипептидные гормоны состоят из небольшого числа аминокис- лот (например, в молекуле тиролиберина их всего три). Однако они синте- зируются в составе гораздо более крупных белков-предшественников, так называемых прогормонов. Так, молекула прогормона для АКТГ — проопио- меланокортина (ПОМК) — состоит из 241 аминокислотного остатка. В ходе процессинга в специализированных клетках передней доли гипофиза (корти- котрофах) из ПОМК образуются АКТГ (39 аминокислотных остатков), более крупный β-липотропин (β-ЛПГ) и другие пепдиды. Исходно синтезируется еще более длинная цепь аминокислот, чем в прогормоне (пре-прогормон). На ее амино-конце присутствует короткий лидерный пептид, «распознающий» компоненты внутриклеточных мембран секреторного пути, что необходимо для правильного проведения прогормона через мембраны шероховатого ре- тикулума клетки. После этого прогормон включается в секреторные гранулы, откуда он выводится в кровь в виде АКТГ и β-ЛПГ. В промежуточной доле гипофиза (функционирующей только у плода и во время беременности) из β-ЛПГ образуются -эндорфин, а из АКТГ — α-МСГ (α- меланоцитостимули- рующий гормон) и полипептид промежуточной доли (CLIP).
Синтез пре-прогормона начинается в ядре эндокринной клетки. Кодирую- щая последовательность гена предшественника полипептидного гормона со- стоит из промоторного участка и собственно транскрибируемой области. Ко- роткие регуляторные последовательности промоторной ДНК способны взаи- модействовать со специфическими ДНК-связывающими белками — усилите- лями (энхансерами) или глушителями (сайленсорами), которые соответствен- но запускают или «гасят» транскрипцию. В ходе транскрипции синтезируются предшественники специфических мРНК, которые подвергаются сплайсингу (вырезанию и соединению значимых нуклеотидных последовательностей).
Образующаяся таким образом мРНК связывается рибосомами, располагаю- щимися в шероховатом ретикулуме цитоплазмы. В цитоплазму из ядра посту- пают и молекулы транспортных РНК (тРНК), которые переносят к рибосомам отдельные аминокислоты, где они встраиваются в последовательность, зако- дированную в нуклеотидной последовательности мРНК (трансляция).
По завершении синтеза молекула пре-прогормона проникает через мем- брану шероховатого ретикулума, теряя при этом лидерный пептид. Прогормон поступает в комплекс Гольджи, где включается в гранулы, перемещающиеся к клеточной мембране. В гранулах присутствуют специфические протеазы, расщепляющие прогормон на составные части. Запасание гормона в грану- лах — основной способ его защиты от внутриклеточной деградации. Другая возможность защиты полипептидных гормонов заключается в их связывании с какой-то молекулой или химическим элементом (например, инсулина с цин- ком) и формировании комплексов, резистентных к цитоплазматическим про- теазам.
Расщепление прогормона с образованием активного гормона не всегда происходит в секреторных гранулах. Так, например, октапептидный гормон ангиотензин II отщепляется от своего прогормона декапептида (ангиотензина I) уже в крови. Однако и сам ангиотензин I образуется не в клетках, а под дей- ствием фермента ренина из белка плазмы ангиотензиногена, который можно рассматривать как пре-прогормон ангиотензина II.
Продукция пептидных гормонов регулируется на различных этапах. На- пример, Т3 ингибирует транскрипцию гена ТТГ и тем самым реализует об- ратную связь в этой эндокринной подсистеме. Глюкоза регулирует продукцию инсулина, влияя не только на его синтез, но и на секрецию за счет индукции слияния секреторных гранул с плазматической мембраной β-клеток. К группе гликопротеидов относятся ТТГ, ЛГ, ФСГ и хорионический гонадотропин. По- разительно, но эти двухцепочечные гормоны, вырабатываемые разными клет- кам и даже разными органами, имеют сходную структуру, при этом структура альфа-цепи идентична у всех гормонов, а в бета-цепи имеются значительные участки гомологии, что создает в ряде случаев уникальные клинические си- туации и обязательно должно учитываться в практике.
Стероидные гормоны
Исходным предшественником стероидных гормонов служит холестерин, в определенном количестве присутствующий во всех клетках, где он либо синтезируется из ацетата, либо поступает из крови в составе липопротеинов. Синтез самих стероидных гормонов в клетках коры надпочечников и гонад протекает в цитоплазме и зависит от активности ряда оксидаз (ферментов цитохрома Р450). Сколько-нибудь значительные запасы стероидных гормо- нов в клетках отсутствуют. Обычно запасаются не сами гормоны, а эфиры холестерина в виде липидных капель. Под влиянием того или иного стиму- ла начинается синтез гормона, который, как правило, сразу же выводится в кровь. Скорость синтеза стероидных гормонов лимитируется первой реакци- ей — отщеплением боковой цепи холестерина с образованием прегненолона. Эта реакция протекает в митохондриях стероидпродуцирующих клеток и ка- тализируется ферментом Р450scc (20,22-десмолазой). Первично регулируется доступность холестерина для этого фермента. Тропные гормоны влияют на транскрипцию гена, кодирующего белок, носящий название «острый регуля- тор стероидогенеза» (StAR), который ускоряет транспорт холестерина через митохондриальную мембрану. Быстрый синтез стероидных гормонов обеспе- чивается активацией предсуществующих ферментов, действующих на моле- кулы предшественников, а долговременная активация предполагает усиление синтеза соответствующих ферментов.
Прочие гормоны
Гормоны, относящиеся к этой группе, зачастую также синтезируются в ходе цитоплазматических ферментативных реакций. Например, тиреоидные гормоны (Т4 и Т3) образуются путем йодирования тирозильных остатков главного белка щитовидной железы — тиреоглобулина. Реакция йодирования катализируется ферментами цитоплазмы или клеточной мембраны. Основная роль в этом процессе принадлежит ферменту тиреопероксидазе (ТПО). После йодирования происходит конденсация йодированных тирозильных остатков с потерей одним из них боковой цепи и соединением двух ароматических колец через атом кислорода.
Под действием цитоплазматических ферментов из предшественника (L-аргинина) образуется и другой гормон этой группы — окись азота.
Витамин D3, подобно стероидам, образуется из холестерина. Под действи- ем ультрафиолетовых лучей холестерин кожи превращается в 7-дегидрохоле- стерин, а затем в холекальциферол. Последний под влиянием митохондриаль- ных ферментов (25-гидроксилазы в печени и 1-гидроксилазы в почках) пре- вращается в активную форму витамина — 1,25(ОН)2D. Скорость образования активного витамина лимитируется реакцией 1-гидроксилирования, и именно эта реакция регулируется ПТГ и фосфатными ионами.
Основным предшественником эйкозаноидов является арахидоновая кис- лота, образующаяся из незаменимой линолевой кислоты, присутствующей в клеточных мембранах. Производными арахидоновой кислоты являются многие сигнальные молекулы — лейкотриены, гидроксиэйкозатетроеновая кислота (HETE) и простагландин Н2 — предшественник других простаглан- динов, простациклинов и тромбоксанов. Содержание того или иного их этих соединений зависит от липидного состава клеточных мембран и активности ферментов, регулируемых различными стимулами.
Формы запасания соответствующих молекул различны. Тироксин, напри- мер, хранится в фолликулах щитовидной железы в составе тиреоглобулина (основного белка коллоида), а продукты мозгового вещества надпочечников запасаются, как и пептидные гормоны, в цитоплазматических секреторных гранулах.
Секреция
Высвобождение любого гормона стимулируется определенными сигнала- ми (так называемое сопряжение возбуждения с секрецией). Они могут быть как высокоспецифическими (например, в отношении секреции паратгормо- на), так и разнообразными (например, в отношении секреции инсулина или альдостерона).
Белковые и полипептидные гормоны выводятся в кровь путем экзоцитоза, предполагающего слияние гранулы с клеточной мембраной и выбрасывание содержимого гранул в кровоток. Как и выделение нейромедиаторов из нерв- ных окончаний, секреция таких гормонов требует присутствия ионов кальция и деполяризации клеточной мембраны (например, в случае инсулина). Стероидные гормоны, как уже отмечалось, практически не накапливаются в клетке и, будучи жирорастворимыми молекулами, сразу же диффундируют через клеточную мембрану. Секреция гормонов смешанной группы осуществляется посредством са- мых разных механизмов — от экзоцитоза (например, катехоламины) до бы- строй диффузии через клеточную мембрану или выщепления из молекулы предшественника (например, Т4).
Скорость секреции многих гормонов обнаруживает отчетливые суточные колебания, связанные с циклом сон-бодрствование. Секреция других гормо- нов (например, гонадотропинов гипофиза) подчиняется эндогенным «биоло-гическим часам», работающим в разных временных шкалах — на протяже- нии отдельных периодов жизни (эмбриональный период, детство, пубертат, детородный период, менопауза), в течение беременности и лактации или мен-струального цикла. Регистрируется также импульсная секреция гормонов с регулярной минутной периодичностью.
Циркуляция в крови
Эффективность доставки гормона к его мишеням зависит от многих фак- торов, включая его свободное или связанное с транспортными белками состо- яние, скорость метаболизма и элиминации из крови. Многие гормоны (в част- ности, стероидные и тиреоидные), попадая в кровь, образуют нековалентные связи с белками плазмы, что может защищать активные молекулы от инакти- вирующих факторов крови и создавать еще один, легкомобилизуемый запас гормонов. Связывание с белками может увеличивать и водорастворимость со- единений, плохо растворяющихся в плазме. Особенно высоким сродством к определенным гормонам обладают, как правило, глобулины (тироксинсвязы- вающий глобулин, транскортин, секс-гормонсвязывающий глобулин, витамин D-связывающий белок). Альбумин обладает низким сродством к гормонам, но высокой емкостью. Свободные гормоны, связывающие белки плазмы и гор- мон-белковые комплексы находятся в состоянии динамического равновесия. При использовании клетками-мишенями большего количества свободного гормона или усилении его элиминации из организма происходит диссоциация большего числа гормон-белковых комплексов, что восстанавливает концен- трацию свободного гормона в крови. При особенно значительной утилизации свободного гормона усиливается уже его секреция эндокринной железой.
Содержание связывающих белков в плазме может меняться, если оно воз- растает, доля свободного гормона уменьшается, что опять-таки приводит к усилению его секреции (еще один пример обратной связи). Общее содержа- ние гормона в крови в этом случае увеличивается, но концентрация активно- го свободного гормона остается нормальной. Например, возрастание уровня белков плазмы при беременности не сопровождается клиническими проявлениями избытка гормонов. Пептидные гормоны в большинстве случаев не связываются с транспортными белками. Исключение составляют ГР, который связывается с белком (идентичным гормонсвязывающему домену рецептора ГР), инсулиноподоб- ные факторы роста (ИФР-1 и ИФР-2), а также АДГ и окситоцин, которые свя- заны с нейрофизинами.
Некоторые гормоны (например, ГР) присутствуют в крови в виде димеров или даже полимеров. При этом мономер ГР биологически гораздо активнее димера. Кроме того, возможна в физиологических условиях циркуляция гор- мона в связи с иммуноглобулином G, это явление наиболее изучено приме- нительно к пролактину, в меньшей степени – ТТГ и кальцитонину. Все эти факты необходимо учитывать при трактовке результатов измерения уровня гормонов в крови.
Гормональная активность модулируется не только секрецией гормонов, но и их трансформацией (конверсией) в периферических тканях (печени, молоч- ных железах, жировой ткани и головном мозге). В результате этого процес- са могут образовываться соединения, обладающие большей или меньшей, а также иной биологической активностью. Например, секретируемый яичками тестостерон в других тканях превращается в более активный дигидротесто- стерон (ДГТ), а периферическая конверсия тироксина (его дейодирование) может приводить к образованию либо более активного Т3, либо биологически неактивного реверсивного Т3 (рТ3). В жировой ткани (и некоторых других) андрогены превращаются в эстрогены, т.е. соединения с совершенно иной биологической активностью.
Разные гормоны действуют в течение разного времени. Если время дей- ствия нейромедиаторов измеряется в среднем миллисекундами, то проста- гландины и пептиды действуют в течение секунд и минут, белки и гликопро- теины — от минут до часов, стероиды — в течение часов, а йодтиронины — на протяжении суток. Большинство пептидных гормонов сохраняется в крови не более нескольких минут. Исключение составляет хорионический гонадо- тропин человека (ХГЧ), t1/2 которого измеряется часами. Основной механизм деградации пептидных гормонов — их связывание с рецепторными и нере- цепторными участками клеточных мембран с последующей интернализацией гормон-белковых комплексов и их разрушением в клетках. Это происходит вследствие слияния лизосом с эндоцитозными пузырьками, содержащими гормон-рецепторные комплексы, и действия на последние кислой среды и ли- зосомных ферментов.
Метаболические превращения стероидных гормонов и витамина D в клет- ках обычно приводят к образованию водорастворимых соединений, выво- димых с мочой. Однако метаболизм стероидов может иметь и регуляторное значение. Так, превращение кортизола в кортизон под действием 11β-гидро- ксистероиддегидрогеназы (11β-ГСД) играет важную роль в регуляции мине- ралокортикоидной активности. Кортизол взаимодействует с минералокорти- коидными рецепторами с высоким сродством; при этом его концентрация в крови в 1000 раз выше концентрации альдостерона. Поэтому превращение кортизола в кортизон защищает почечные минералокортикоидные рецепторы от чрезмерной активации. Генетические дефекты 11β-ГСД обусловливают со- стояние кажущегося избытка минералокортикоидов.
Из стероидов андростендиона и дегидроэпиандростерона (ДГЭА) может образовываться тестостерон, а из него в тканях-мишенях — эстрадиол и ди- гидротестостерон.
Период полужизни тиреоидных гормонов в крови составляет примерно 7 суток для Т4 и одни сутки для Т3. Под действием минимум трех разных дейодиназ (содержание которых в разных тканях различно) от этих гормонов отщепляются атомы йода. Дейодирование наружного кольца тиронина пре- вращает малоактивный Т4 в более активный Т3. Другие реакции дейодиро- вания инактивируют тиреоидные гормоны. Метаболизм последних включает также дезаминирование боковой цепи и конъюгирование с глюкуроновой или серной кислотой.
Таким образом, периферический метаболизм гормонов обеспечивает до- полнительную возможность регуляции гормональных эффектов.
Механизмы действия гормонов
Механизмы действия разных гормонов при всем их различии имеют ряд общих признаков. Первая стадия, на которой происходит «узнавание» гормо- ном своих клеток-мишеней, высоко специфична и обусловлена присутствием в клетках высоко аффинных рецепторов. Последние связаны с сигнальными эффекторными системами, которые и обусловливают видимые реакции на гормон.
Рецепторы — это белки, содержащие специфические участки связывания того или иного соединения. Все соединения, связывающиеся с данным ре- цептором, называются его лигандами. В зависимости от функционального результата лиганд-рецепторного взаимодействия различают агонисты и анта- гонисты рецепторов. Агонисты активируют эффекторные механизмы и ини- циируют биологическую реакцию, тогда как антагонисты, хотя и связывают- ся с рецептором, но не активируют эффекторные механизмы и препятствуют взаимодействию рецептора с агонистами.
В ряде тканей число рецепторов многократно превышает необходимое для реализации максимальной биологической реакции. При недостаточно насы- щающих концентрациях лиганда это обеспечивает формирование лиганд-ре-цепторных комплексов, достаточных для полной активации внутриклеточных эффекторных систем.
Распознавание рецептора гормоном (или наоборот) может происходить как на клеточной мембране, так и во внутренней среде клетки.
Для белковых и полипептидных гормонов клеточная мембрана, как пра- вило, непроницаема, и они должны прежде всего взаимодействовать с рецеп- торами плазматической мембраны. Это взаимодействие обусловливает об- разование так называемых «вторых посредников» передачи сигнала (первым считается сам гормон). В то же время полипептидные гормоны в комплексе со своими поверхностными рецепторами способны проникать внутрь клеток- мишеней путем эндоцитоза (интернализация), что может быть одним из эта- пов инактивации гормона.
Жирорастворимые молекулы (например, стероиды) проникают сквозь ли- пидный слой клеточных мембран путем простой диффузии и удерживаются во внутренней клеточной среде за счет взаимодействия со специфическими цитоплазматическими или ядерными белками (рецепторами). Взаимодействие гормона с рецептором изменяет аллостерическую конфи- гурацию последнего, придавая ему биологическую активность. Это взаимо- действие подчиняется закону действия масс. Сродство гормона к своему ре- цептору отражает отношение скоростей образования и диссоциации гормон- рецепторного комплекса. При быстром образовании и быстрой диссоциации такого комплекса интенсивность гормонального сигнала определяется кон- центрацией гормона (как при действии нейротрансмиттеров), тогда при бол медленных процессах эффект поддерживается активированным рецептором.
Рецепторы клеточной мембраны
Поверхностные клеточные рецепторы — один из видов многочисленных мембранных молекул, находящихся в очень сложном взаимодействии друг с другом. В структуре таких рецепторов различают лигандсвязывающий до- мен, расположенный на наружной поверхности клеточной мембраны, один или несколько внутримембранных доменов и регулируемый лигандом цито- плазматический «эффекторный» домен. Такая структура обеспечивает воз- можность восприятия клеткой внеклеточных сигналов и их проведения во внутриклеточную среду.
Серпентиновые рецепторы с семью трансмембранными доменами (со- пряженные с G-белками) опосредуют эффекты катехоламинов, простаглан- динов, большинства тропных гормонов гипофиза, глюкагона и др. За наруж- ным лигандсвязывающим N-концевым доменом этих рецепторов следуют ги- дрофобные аминокислотные последовательности, семь раз пронизывающие липидный бислой клеточной мембраны (семь внутримембранных доменов), и цитоплазматический гидрофильный C-концевой домен. Ко второму типу принадлежат рецепторы с одним трансмембранным доменом, обладающие собственной тирозинкиназной активностью (рецепторы инсулина, ИФР, эпи-дермального фактора роста и др.). Рецепторы третьего типа характеризуются крупным внеклеточным и тоже одним трансмембранным доменом с цитоплаз- матическим хвостом. Эти рецепторы лишены собственной тирозинкиназной активности и реализуют свою функцию, взаимодействуя с растворимыми молекулами (трансдукторами), обладающими ферментативной активностью. Эта группа включает рецепторы ПРЛ и ГР. Наконец, рецепторы четвертого типа (к которым относится, в частности, рецептор натрийуретического пеп- тида) ковалентно связаны с гуанилатциклазой, являющейся частью рецептор- ной молекулы.
Каждый G-белок состоит из трех субъединиц α, β и Y. При взаимодействии G-белка с рецептором α-субъединица отсоеди- няется от димерной β/Y-субъединицы и в зависимости от того, образовалась ли она из Gs- или Gi-белка, либо стимулирует, либо ингибирует сопряженную с G-белком каталитическую единицу. Последняя представляет собой фермент (аденилатциклазу, гуанилатциклазу, фосфолипазу С и т.п.). В результате и об- разуются «вторые посредники» (вторичные мессенджеры), инициирующие изменение активности внутриклеточных ферментов и транскрипцию генов.
В неактивированном G-белке α-субъединица связана с ГДФ. Присоедине- ние к рецептору лиганда-агониста обусловливает физический контакт между рецептором с распознающим его G-белком, вследствие чего α-субъединица меняет ГДФ на ГТФ (концентрация которого в клетке значительно выше кон- центрации ГДФ). Именно связывание α-субъединицей ГТФ приводит к ее диссоциации от димерной β/Y-субъединицы. Одновременно диссоциирует и гормон-рецепторный комплекс. Продолжительность активации эффекторов определяется собственной ГТФ-азной активностью α-субъединицы. Превра- щение ГТФ в ГДФ лишает α-субъединицу активности и приводит к реассоци- ации тримерного G-белка, возвращая систему в исходное состояние.
Среди эффекторов, активируемых Gs-белками, чаще других упоминается аденилатциклаза, увеличивающая внутриклеточный уровень циклическо- го аденозинмонофосфата (цАМФ). Последний связывается с ингибиторной регуляторной субъединицей неактивной протеинкиназы А (ПКА), приводя к отсоединению этой субъединицы и высвобождению активной каталитиче- ской субъединицы фермента, которая фосфорилирует (и тем самым активи- рует) различные субстраты. К ним принадлежит белок, связывающий цАМФ- чувствительный элемент ДНК (CREB) и другие факторы транскрипции.
Современные успехи молекулярной биологии, генетики, а также клиниче- ских дисциплин настолько усложнили общее понимание эндокринологии, что обусловили необходимость ее деления на ряд самостоятельных, хотя и объ- единенных общими принципами медико-биологических дисциплин — нейроэн- докринологию, диабетологию, тиреоидологию, эндокринологию репродукции и т.п. Более детальные знания основ каждой из этих дисциплин должно дать описание механизмов конкретных эндокринных заболеваний.
Оценка физического и полового развития
Т.Ю. Ширяева, Е.В. Нагаева, О.Б. Безлепкина
Физическое развитие — динамический процесс роста (увеличение длины и массы тела, развитие органов и систем организма) и биологического созре- вания ребёнка в определённом периоде детства. В основе оценки физического развития лежат параметры роста, массы тела, пропорции отдельных частей тела и степень развития функциональных способностей организма (физиче- ская подготовленность). Только при их совместном рассмотрении можно дать объективную оценку физического развития.
Оценка физического развития
Цель — определить:
• «нормально» ли физически развивается ребенок;
• имеет ли он аномалию развития или тенденцию к возникновению анома- лии физического развития, которую необходимо устранить.
Алгоритм действий:
• правильное измерение массы тела, длины тела (роста);
• расчет ИМТ;
• нанесение результатов измерений на графики массы тела/роста, интер- претация полученных данных с учетом возраста и половой принадлежно- сти ребенка;
Правильное измерение, построение графиков и интерпретация антропоме- трических данных имеют первостепенное значение для выявления проблем физического развития ребенка.
Оценка физического развития детей по нормам ВОЗ
ВОЗ были разработаны нормы физического развития, имеющие силу предписания, а не просто эталонного значения описательного характера. Новые нормы показывают, какое физическое развитие может быть достигнуто при обеспечении оптимальных условий для развития ребенка, в частности, со-блюдении рекомендаций по кормлению и медико-санитарному уходу (напри- мер проведение профилактических прививок, уход во время болезни).
Преимущества оценки физического развития детей по нормам ВОЗ:
• в качестве образца здорового роста и развития приняты дети грудного возраста, находящиеся на грудном вскармливании;
• новые нормы, в частности ИМТ, полезны для оценки растущей всемир- ной эпидемии ожирения;
• графики, показывающие стандартные модели ожидаемых темпов роста
по оси времени, позволяют медицинским работникам раньше выявлять де- тей, имеющих тенденцию аномального роста, которым угрожает недостаточ- ное питание или ожирение, не дожидаясь возникновения явной аномалии;
• стандарты ВОЗ описывают нормальный рост детей в оптимальных эко- логических условиях, их можно использовать для оценки детей независи- мо от этнической принадлежности, социально-экономического статуса и типа кормления.
Основные положения правильного измерения длины тела (роста) ребенка
В зависимости от возраста ребенка и его способности стоять измеряют длину тела или рост ребенка. Длина тела ребенка измеряется в положении лежа, рост — в положении стоя. Обычно рост в положении стоя примерно на 0,7 см меньше, чем длина тела в положении лежа. Эта разница была учтена при разработке норм роста ВОЗ. Поэтому важно вносить поправку в измерения, если вместо роста используется длина тела и наоборот.
Если ребенок до 2 лет не захочет лечь для измерения длины, измеряют рост в положении стоя и прибавляют 0,7 см, чтобы преобразовать рост в длину тела. Если ребенок в возрасте 2 лет или старше не может стоять, измеряют дли- ну тела в положении лежа и вычитают 0,7 см, чтобы преобразовать длину тела в рост.
Для измерения длины тела ребенка необходима мерная доска (ростомер для детей грудного возраста), которая кладется на плоскую устойчивую поверх- ность, например, на стол.
Для измерения роста используют ростомер, устанавливаемый под прямым углом между ровным полом и прямой вертикальной поверхностью, такой как стена.
Методика измерения длины тела лежа
В целях гигиены и для удобства ребенка ростомер для детей грудного воз- раста накрывают тонкой материей или мягкой бумагой. Мать должна сама положить ребенка на спину на ростомер, а затем, стоя напротив медработника с другой стороны ростомера, держать его голову у неподвижного надголовни- ка, пока медработник будет производить измерение.
Голова ребенка должна располагаться так, чтобы воображаемая вертикаль- ная линия от ушного канала до нижней границы глазницы проходила пер- пендикулярно к ростомеру (глаза ребенка должны быть направлены прямо верх). Мать должна встать у изголовья и удерживать голову ребенка в таком положении.
Следует убедиться, что ребенок лежит ровно и не меняет своего положе- ния. Плечи должны касаться горизонтальной поверхности, спина не должна выгибаться.
Одной рукой прижимают ноги ребенка, мягко надавливая на колени, чтобы максимально выпрямить ноги, а другой рукой перемещают подножку.
У новорожденных невозможно выпрямить колени в той же степени, как у детей постарше. Ввиду легкой ранимости, надавливание на колени у ново- рожденных должно быть минимальным.
Если ребенок слишком возбужден и невозможно удержать обе ноги в од- ном положении, измерение производят с одной ногой в нужном положении.
Удерживая колени, до упора подвигают подножку к ногам ребенка. Подо- швы стоп ребенка должны лежать ровно на подножке, пальцы ног должны быть направлены вверх.
Необходимо снять показание и записать длину тела ребенка в сантиметрах с точностью до 0,1 см.Чтобы правильно измерить длину, все действия необ- ходимо проводить быстро и уверенно, пока ребенок не начал капризничать.